Rifaximin-α reduziert effektiv das Auftreten wiederkehrender HE-Episoden.1, 2, * Zusätzlich wird mit Rifaximin-α das Risiko für weitere Komplikationen signifikant verringert,3, 4, §, &, + was zu einem signifikant verlängerten Gesamtüberleben führt.3, §, & Weiterhin zeigt Rifaximin-α in Studien eine Senkung der Gesundheitskosten, eine Verbesserung der Lebensqualität und eine hohe Compliance – auch in der Langzeitanwendung.6 – 9,#
Rifaximin-α, der moderne Behandlungsstandard
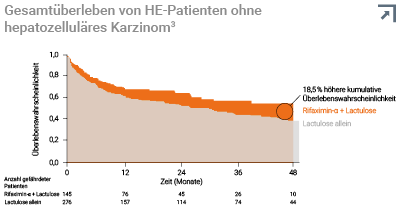 In einer retrospektiven Analyse von 1.042 HE-Patienten wurde die
In einer retrospektiven Analyse von 1.042 HE-Patienten wurde die
Wirkung einer Rifaximin-α-Behandlung auf das Gesamtüberleben
und das Auftreten verschiedener Komplikationen der Leberzirrhose
untersucht.3, &
- In der Kohorte ohne hepatozelluläres Karzinom (n = 421) zeigte
sich eine signifikante Reduktion des Mortalitätsrisikos unter
Behandlung mit Rifaximin-α + Lactulose verglichen zu Lactulose
allein.3, & - Zudem verringerte Rifaximin-α bei diesen Patienten signifikant das
Risiko für Komplikationen der Leberzirrhose (wiederkehrende HE-Episoden,
spontan bakterielle Peritonitis und Varizenblutungen).3, &
STUDIENDETAILS
Rifaximin treatment is associated with reduced risk of cirrhotic complications and prolonged overall survival in patients
experiencing hepatic encephalopathy
Kang SH, et al. Aliment Pharmacol Ther 2017; 46: 845–55.
Retrospektive Studie
Untersuchung von 1.042 HE-Patienten: Von diesen litten 621 Patienten an hepatozellulärem Karzinom (HCC), 421 wiesen kein
HCC auf. In der Kohorte ohne HCC erhielten 145 Patienten Rifaximin-α + Lactulose, 276 Patienten bekamen nur Lactulose. In
der HCC-Kohorte erhielten 173 Patienten Rifaximin-α + Lactulose und 448 Patienten nur Lactulose. Die jeweiligen Dosierungen
lagen bei Rifaximin-α 600 mg 2x täglich sowie 30–60 ml Lactulose 3x täglich.3
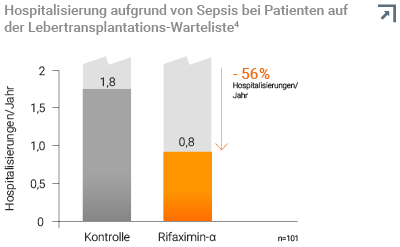
Die Krankenhausdaten von HE-Patienten auf der Lebertransplantationsliste
wurden retrospektiv über einen Zeitraum von zwei Jahren ausgewertet. Patienten mit mindestens zwei zurückliegenden HE-Episoden oder einer akuten HE-Episode zum Zeitpunkt der Transplantationsbeurteilung wurden eingeschlossen.4, +
Bei HE-Patienten, die mit Rifaximin-α behandelt wurden, zeigte sich
eine signifikante Reduktion der Hospitalisierungen aufgrund von
Sepsis.4, +
STUDIENDETAILS
Rifaximin reduces the incidence of sepsis and all-cause admissions whilst on the liver transplant waiting list
Salehi, S. et al. J Hepatol 2018; 68(Suppl 1):S119–20. Abstract LBP-027.
Retrospektive Analyse
Analyse der Krankenhausdaten von 101 HE-Patienten auf der Lebertransplantationsliste mit und ohne Rifaximin-α-Prophylaxe.
Von den 101 HE-Patienten wurden 66 mit Rifaximin-α behandelt und 35 Patienten nicht. 82 % der Patienten unter Rifaximin-α
und 71 % der Patienten ohne Rifaximin-α erhielten begleitend Lactulose.4
STUDIENDETAILS
Rifaximin Treatment in Hepatic Encephalopathy.
Bass et al. N Engl J Med. 2010 Mar 25; 362(12):1071–81.8.
Randomisierte, doppelblinde, Placebo-kontrollierte Phase-III-Studie.
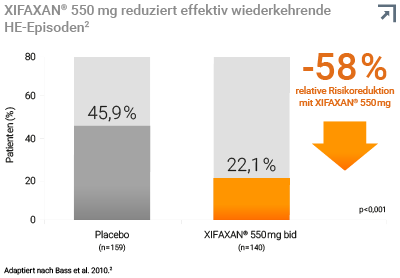
299 Patienten mit chronischer Lebererkrankung in Remission einer HE (Grad ≤ 1) und mindestens 2 wiederkehrenden HE-Episoden in den letzten 6 Monaten (Grad ≥ 2). Davon erhielten 140 Patienten XIFAXAN® 550 mg 2-× tägl. und 159 Patienten Placebo. Behandlungszeitraum: 6 Monate (> 90 % in beiden Behandlungsarmen erhielten zusätzlich Lactulose).2
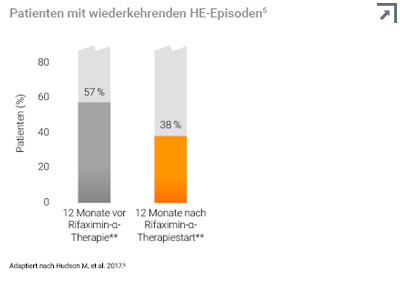 In einer multizentrischen, retrospektiven Beobachtungsstudie wurden 207 Patienten mit Hepatischer Enzephalopathie aus 13 Zentren des National Health Service im Vereinigten Königreich eingeschlossen. Bei allen diesen Patienten wurde zwischen Juli 2008 und Mai 2014 eine Behandlung mit Rifaximin-α eingeleitet.5, **
In einer multizentrischen, retrospektiven Beobachtungsstudie wurden 207 Patienten mit Hepatischer Enzephalopathie aus 13 Zentren des National Health Service im Vereinigten Königreich eingeschlossen. Bei allen diesen Patienten wurde zwischen Juli 2008 und Mai 2014 eine Behandlung mit Rifaximin-α eingeleitet.5, **
Vergleicht man das Auftreten wiederkehrender HE-Episoden 12 Monate vor Rifaximin-α-Therapie und 12 Monate nach Therapiestart, zeigt sich eine signifikante Reduktion.5
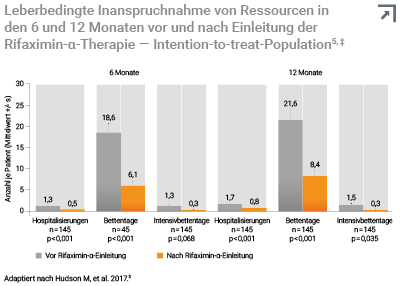 Daten zum Krankenhausressourcenverbrauch standen bei 145 der
Daten zum Krankenhausressourcenverbrauch standen bei 145 der
207 Patienten zur Verfügung. Folgende signifikante Veränderungen wurden beim Vergleich der 6 Monate vor und nach Einleitung der Rifaximin-α-Therapie bei den Patienten, die zum Ende des Beobachtungszeitraums noch lebten, festgestellt:5
- eine Abnahme der mittleren Zahl der Hospitalisierungen/Patient
- eine Abnahme der Krankenhausbettentage/Patient
- eine Verringerung der stationären Wiederaufnahmen innerhalb von 30 Tagen/Patient
- eine Verringerung der Notaufnahmebesuche/Patient
- eine Abnahme der Intensivbettentage/Patient
STUDIENDETAILS
The impact of rifaximin-α on the hospital resource use associated with the management of patients with hepatic encephalopathy: a retrospective observational study (IMPRESS)Mullen et al. Hudson, M et al. Frontline Gastroenterol 2017; 8(4): 243–51.
Multizentrische, retrospektive Beobachtungsstudie
Untersucht wurde der Einfluss einer HE-Therapie mit Rifaximin-α auf die Krankenhausressourcen. Eingeschlossen wurden insgesamt 207 Patienten, bei denen zwischen Juli 2008 und Mai 2014 eine Behandlung mit Rifaximin-α eingeleitet wurde (Tagesdosen von 1100 mg bzw. 1200 mg Rifaximin-α). Daten zum Ressourcenverbrauch standen bei 145 der 207 Patienten zur Verfügung.5
Reduktion der HE-bedingten Hospitalisierungen2,7,*,#
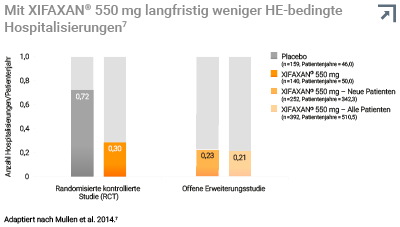 In einer 6-monatigen Placebo-kontrollierten Studie reduzierte sich bei Behandlung mit XIFAXAN® 550 mg das relative Risiko für HE-bedingte Hospitalisierungen um 50 %.2,*
In einer 6-monatigen Placebo-kontrollierten Studie reduzierte sich bei Behandlung mit XIFAXAN® 550 mg das relative Risiko für HE-bedingte Hospitalisierungen um 50 %.2,*
Auch in einer Langzeitstudie mit XIFAXAN® 550 mg wurde eine Reduktion der Rate der HE-bedingten Hospitalisierungen sowie der Hospitalisierungen insgesamt gezeigt, ohne dass sich dabei die Rate unerwünschter Ereignisse erhöhte. Zum Vergleich der Langzeitwirkung wurden die Werte der Patienten aus der 6-monatigen randomisierten Kontrollstudie herangezogen.7,#
Klarer Vorteil bei Anzahl, Aufenthaltsdauer und Kosten von Hospitalisierungen8
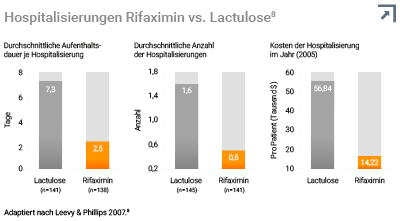 Im Vergleich zur Lactulose-Therapie führte Rifaximin zu weniger Hospitalisierungen, einer kürzeren Aufenthaltsdauer und geringeren jährlichen Hospitalisierungskosten.8
Im Vergleich zur Lactulose-Therapie führte Rifaximin zu weniger Hospitalisierungen, einer kürzeren Aufenthaltsdauer und geringeren jährlichen Hospitalisierungskosten.8
Mehr Erlös durch verkürzte Liegedauer8
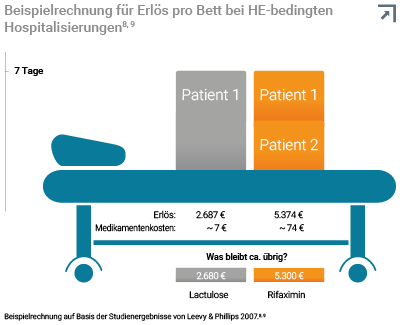 In einer Studie konnte gezeigt werden, dass die Liegedauer für einen HE-Patienten unter Rifaximin, verglichen mit Lactulose, um etwa die Hälfte reduziert werden kann. Für den Klinikalltag bedeuted das: Das Bett wird schneller wieder frei und kann mit einem neuen Patienten belegt werden. Höhere Medikamentenkosten für Rifaximin werden so kompensiert und Krankenhäuser können ihre Erlöse steigern.8
In einer Studie konnte gezeigt werden, dass die Liegedauer für einen HE-Patienten unter Rifaximin, verglichen mit Lactulose, um etwa die Hälfte reduziert werden kann. Für den Klinikalltag bedeuted das: Das Bett wird schneller wieder frei und kann mit einem neuen Patienten belegt werden. Höhere Medikamentenkosten für Rifaximin werden so kompensiert und Krankenhäuser können ihre Erlöse steigern.8
STUDIENDETAILS
Rifaximin Is Safe and Well Tolerated for Long-Term Maintenance of Remission From Overt Hepatic Encephalopathy.
Mullen et al. Clin Gastroenterol Hepatol. 2014 Aug; 12:1390–97.
Offene Erhaltungsstudie.
322 Patienten mit HE-Episoden innerhalb der letzten 12 Monate (Grad ≥ 2) und einem derzeitigen Grad von höchstens 2 erhielten XIFAXAN® 550 mg 2-× tägl., einschließlich der Patienten aus der 6-monatigen randomisierten, kontrollierten Studie (RCT). 89,8 % der Patienten erhielten begleitend Lactulose. Dabei wurden Sicherheits- und Hospitalisierungsdaten bei den Patienten verglichen, die in der RCT Placebo bzw. Rifaximin erhielten.7
Hospitalizations during the use of Rifaximin versus Lactulose for the Treatment of Hepatic Encephalopathy
Leevy & Phillips Dig Dis Sci. 2007 Mar;52(3):737–41
Retrospektive Studie.
145 Krankenakten zu Patienten mit Hepatischer Enzephalopathie, die Lactulose 30 ml 2-× tägl. für ≥ 6 Monate und anschließend Rifaximin 400 mg 3 × tägl. ≥ 6 Monate erhielten. Verglichen wurden die letzten 6 Monate unter Lactulose-Therapie mit den ersten 6 Monaten unter Rifaximin-Therapie. 8
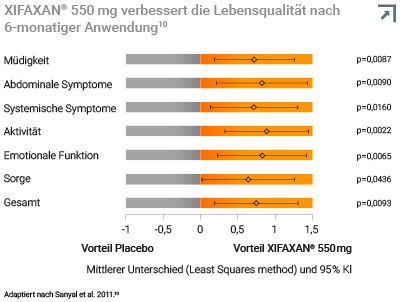 XIFAXAN® 550 mg verbesserte signifikant die Lebensqualität bei Patienten mit Leberzirrhose in Remission einer HE und mit vorherigen wiederkehrenden HE-Episoden. Die Lebensqualität wurde anhand des Fragebogens zu chronischen Lebererkrankungen (Chronic Liver Disease Questionnaire (CLDQ)) ermittelt. In der Studie zeigte sich, dass sich die Werte durch Rifaximin in allen abgefragten Kategorien des CLDQ signifikant verbesserten.10
XIFAXAN® 550 mg verbesserte signifikant die Lebensqualität bei Patienten mit Leberzirrhose in Remission einer HE und mit vorherigen wiederkehrenden HE-Episoden. Die Lebensqualität wurde anhand des Fragebogens zu chronischen Lebererkrankungen (Chronic Liver Disease Questionnaire (CLDQ)) ermittelt. In der Studie zeigte sich, dass sich die Werte durch Rifaximin in allen abgefragten Kategorien des CLDQ signifikant verbesserten.10
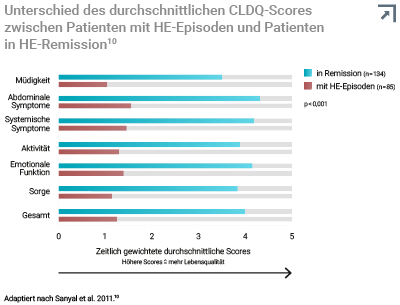 Eine niedrigere Lebensqualität könnte dabei einen Prädikator für wiederkehrende HE-Episoden darstellen, denn laut CLDQ wirken sich HE-Episoden negativ auf die Lebensqualität aus.10
Eine niedrigere Lebensqualität könnte dabei einen Prädikator für wiederkehrende HE-Episoden darstellen, denn laut CLDQ wirken sich HE-Episoden negativ auf die Lebensqualität aus.10
STUDIENDETAILS
Sanyal et al. Aliment Pharmacol Ther. 2011 Oct; 34(8):853-61.
Randomised clinical trial: rifaximin improves health related quality of life in cirrhotic patients with hepatic encephalopathy – a double-blind placebo-controlled study.
Multizentrische Phase-III-Studie.
219 Patienten mit Leberzirrhose in Remission einer HE (Grad = 0 oder 1) und wiederkehrenden Durchbruchsepisoden in der Anamnese (≥ 2 in 6 Monaten). Davon erhielten 101 Patienten XIFAXAN® 550 mg 2-× tägl. und 118 Patienten Placebo. Behandlungszeitraum: 6 Monate.10
 In einer Langzeitstudie mit XIFAXAN® 550 mg konnte bei HE-Patienten ein hohes Maß an Therapie-Compliance erreicht werden: 92,2 % der Patienten zeigten eine Adhärenz ≥ 80 %.7,#
In einer Langzeitstudie mit XIFAXAN® 550 mg konnte bei HE-Patienten ein hohes Maß an Therapie-Compliance erreicht werden: 92,2 % der Patienten zeigten eine Adhärenz ≥ 80 %.7,#
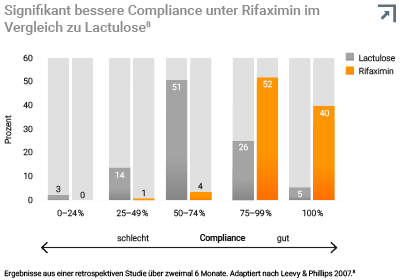
In einer Vergleichsstudie zeigte sich außerdem, dass bei den gleichen Patienten die Compliance mit Rifaximin-Therapie signifikant höher ist als unter der Einnahme von Lactulose.8
STUDIENDETAILS
Rifaximin Is Safe and Well Tolerated for Long-Term Maintenance of Remission From Overt Hepatic Encephalopathy
Mullen et al. Clin Gastroenterol Hepatol. 2014 Aug; 12:1390–97.
Offene Erhaltungsstudie.
322 Patienten mit HE-Episoden innerhalb der letzten 12 Monate (Grad ≥ 2) und einem derzeitigen Grad von höchstens 2 erhielten XIFAXAN® 550 mg 2-× tägl., einschließlich der Patienten aus der 6-monatigen randomisierten, kontrollierten Studie (RCT). 89,8 % der Patienten erhielten begleitend Lactulose. Dabei wurden Sicherheits- und Hospitalisierungsdaten bei den Patienten verglichen, die in der RCT Placebo bzw. Rifaximin erhielten.7
Hospitalizations during the use of Rifaximin versus Lactulose for the Treatment of Hepatic Encephalopathy
Leevy & Phillips Dig Dis Sci. 2007 Mar;52(3):737–41.
Retrospektive Studie.
145 Krankenakten zu Patienten mit HE, die Lactulose 30 ml 2-× tägl. für ≥ 6 Monate und anschließend Rifaximin 400 mg 3-× tägl. ≥ 6 Monate erhielten. Verglichen wurden die letzten 6 Monate unter Lactulose-Therapie mit den ersten 6 Monaten unter Rifaximin-Therapie.8
* Bass et al.: In den Studien zu Rifaximin-α vs. Lactulose alleine, erhielten 91 % der Patienten neben Rifaximin-α auch Lactulose als Begleitmedikation. / § Kang et al.: Bei HE-Patienten ohne hepatozelluläres Karzinom. / & Kang et al.: Patienten erhielten neben Rifaximin-α auch Lactulose als Begleitmedikation; Patienten erhielten 1200 mg Rifaximin/Tag. / + Salehi et al.: 82 % der Patienten in der Rifaximin-α-Gruppe und 71 % der Patienten in der Kontrollgruppe erhielten Lactulose als Begleitmedikation. / # Mullen et al.: Behandlungsdauer von bis zu 24 Monate; 89,8 % der Patienten erhielten als Begleitmedikation Lactulose. / ** 34 % der Patienten erhielten 1100 mg Rifaximin-α/Tag. 61 % erhielten 1200 mg Rifaximin-α/Tag und 5 % erhielten andere Rifaximin-α-Dosen. / ‡ In dieser Analyse wurden die Daten aller zu Studienbeginn eingeschlossenen Patienten berücksichtigt, einschließlich der Daten verstorbener Patienten.
1. XIFAXAN® 550 mg Fachinformation. / 2. Bass NM, et al. N Engl J Med 2010; 362(12): 1071–81. / 3. Kang SH, et al. Aliment Pharmacol Ther 2017; 46: 845–55. / 4. Salehi, S. et al. J Hepatol 2018; 68(Suppl 1):S119–20. Abstract LBP-027. / 5. Hudson, M et al. Frontline Gastroenterol 2017; 8(4): 243–51. / 6.Vilstrup et al. J Hepatol. 2014; 61(3): 642 59 / 7. Mullen et al. Clin Gastroenterol Hepatol. 2014; 12:1390–97. / 8. Leevy & Phillips Dig Dis Sci. 2007; 52(3):737–41. / 9. Web Grouper, DRG Research Group Uniklinikum Münster GDRG 2015 | Fallpauschalenkatalog INEK. / 10. Sanyal et al. Aliment Pharmacol Ther. 2011; 34(8):853–61. / 11. Aspinall RJ, et al. Frontline Gastroenterology 2022; 0: 1–8.